((این تحقیق شامل 66 صفحه همراه با عکس می باشد که بسیار تحقیق کاملی می باشد و در فرمت ورد می باشد.
برای اطمینان از کامل بودن تحقیق لطفا فهرست را مطالعه کنید و مطالب پایین صفحه را مطالعه بفرمایید.))
خرید تحقیق کامل استخراج مس باحلال و بیولیچینگ
(همچنین در این تحقیق گزارشی از کاکرد لیچینگ مجتمع مس میدوک و مس سرچشمه نوشته شده است)
(تحقیق شامل 66 صفحه با فرمت ورد است)قیمت فقط 50هزارتومان
نمونه ای از مطالب داخل تحقیق:
استخراج با حلال وبيوليچينگ
فهرست
مقدمه …………………………………………………………………………………………………………………………………………………………………….2
تاريخچه استخراج فلزات به روش هيدرومتالورژي……………………………………………………………….………………………….……………………………….3
1-2- مزايای روش هيدرو متالوژی ……………………………………………………………………………………………..……………………………………………3
1-3- معا يب روش هيدرو متالوژی ……………………………………………………………………………………………..……………………………..………5
1-4- تاريخچه استخراج مس به روش استخراج با حلال……………………………………………………………………………………………………………5
مزاياي روش SX/EW ……………………………………………………………………………………………………………………………………………………
2- استخراج فلزات به روش هيدرومتالورژي………………………………………………………………………..………………………..………………………………6
2-1-انحلال سنگ معدن……………………….………………………………………………………………………………………………………………………………..6
2-1-1- روشهاي انحلال سنگ معدن :………………………………………………………………………..………………………….…………..……………………..6
آماده سازي جامد:……………………………………….………………………………………………………………………………………………………………………9
استخراج از جامدات بصورت توده اي :………………………………………………………………………………………………………………………………………..9
واحد انحلال توده ای( HEAP LEACHING) در مس سرچشمه……………………..…………………………………………………………………………………10
2-2-1- هيپ و سيستم جمع آوری زيرهيپ :…………………..…………………………………………………………………………………………………………10
2-2-3- هيپ و سيستم پاشش روی هيپ:………………………………………………………………………………………………………………………………..11
2- فرآيند استخراج با حلال : (Solvent Extraction )…………………….……………………………………………………………………………………………..12
2-1- شيمي فرآيند استخراج با حلال :………………………………………………………………………….……………………………………………………..…….14
2-2- سينتيك فرآيند استخراج باحلال :……………………..………………………………………………………………………………………………………………..16
3- مواد مصرفي درفرآيند استخراج باحلال (SOLVENT EXTRACTION ) :……………….…………………………………………………………………………..17
3-1- استخراج كننده هاي مصرفي در فرايند استخراج باحلال:……………..……………………………………………………………………………………………17
3-1-1- خصوصيات يك استخراج كننده مطلوب در فرايند استخراج باحلال:……………….…………………………………………………………………………….17
3-1-2-شيمي تجزيه اكسيم در واحدهاي استخراج با حلال ( SX ) :……………..……………………………………………………………………………………17
3-1-2-1- تجزيه اكسيمها :………………………………………………………………………………………………………………………………………………………19
الف- هيدروليز اكسيمها :…………………………………………………………………………………………………………………………………………………………19
ب- نيتراسيون :…………………………………………………………………………………………………………………………………………………………………….22
د- سولفوناسيون :……………………………………………………………………………………………………………………………………………………………….27
3-2- رقيق كننده هاي مصرفي در فرآيند استخراج با حلال:………………..…………………………………………………………………………………………….27
3-2-1- خصوصيات عمومي يك رقيق كننده مطلوب در فرآيند استخراج با حلال :…………….……………………………………………………………………….28
3-2-2- هدف از افزودن رقيق كننده به فاز آلي :………………………………………………………………………………………………. ……………………………29
3-2-3- منبع تهيه رقيق كننده ها:……………………………………………………………………………………………………………………………………………….30
3-2-4- بررسي خواص فيزيكي رقيق كننده :………………..……………………………………………………………………………………………………………….32
ه- كشش سطحي ………………………………………………………………………………………………………………………………………………………37
و – خاصيت امو لسيون ( Emul esion ) ……………………..……………………………………………………………………………………………………………….38
3-2-5- بررسي خواص انواع حلالهاي نفتي مورد استفاده در صنعت………………………………………………………………………………..…………………….38
3-2- 6- تاثير حلاليت تركيبات فاز آلي در فرآيند استخراج با حلال…………………………………………………………………………………….……………………40
3-2-7- تاثير قطبيت رقيق كننده بر استخراج فلزات…………………………………………………………………………………………………………………………..41
3-2- 8- تاثير درصد تركيبات آروماتيك بر عملكرد رقيق كننده:…………………………………………………………………………………………………………….41
3-3 – تلفات رقيق كننده واستخراج كننده…………………..………………………………………………………………………………………………..………………….43
3-3-1- تلفات رقيق كننده ناشي از ماندگي فازي………………………………………………………………………………………………………………………………44
3-3-2- تلفات رقيق كننده ناشي از تبخير…………………………………………………………………………………………………………………………………………44
3-3-3- تلفات رقيق كننده ناشي از تشكيل كراد……………………………………………………………………………………………..…………………………………47
4- كراد چيست …………………….…………………………………………………………………………………………………………………………………………………..48
4-2-عواملي كه ممكن است در تشكيل كراد موثر باشند: ……………………………………………………………………………………………………………………..48
4-2-1- طبيعت خوراك ( Nature of feed ) …………………….………………………………………………………………………………………..……………………..48
4-2-2- طبيعت استخراج كننده ……………………..…………………………………………………………………………………………………………….………………….49
4-2-3- انتخاب دستگاه………………………………………………………………………………………………………………………………………………………….49
4-2-4- روش عملياتي……………………………………………………………………………………………………………………………………………………………50
4-3- سيليس واثر آن برتشكيل كراد…………………………………………………………………………………………………………………………………………..51
4-3-1- خواص سيليس…………………………………………………………………………………………………………………………………………………………..51
4-3-2- انواع سيليس:……………………………………………………………………………………………………………………………………………………………52
4-3-3- واكنشهاي ناهمگن………………………………………………………………………………………………………………………………………………………53
4-3-4- رسوب مولكولي………………………………………………………………………………………………………………………………………………………….54
4-3-5-پليمريزاسيون……………………………………………………………………………………………………………………………………………………………..54
4-3-6- واكنش هاي آلي…………………………………………………………………………………………………………………………………………………………55
4-8-ماهيت كراد…………………………………………………………………………………………………………………………………………………………………..56.
4-4- توصيف بعضي از كراد ها……………………………………………………………………………………………………………………………………………………57
4-7- اثر كراد بر عمليات واحدهاي استخراج با حلال…………………………………………………………………………………………………………………………..58
4-1-پيشرفت كراد در يك واحد SX باعث بروز مشكلات ذيل ميگردد:………………………………………………………………………………………………………..59
4-6- جلوگيري از تشكيل كراد…………………………………………………………………………………………………………………………………………………….62
4-7- كنترل و تخليه كراد……………………………………………………………………………………………………………………………………………………………64
4-5- طرز عمل و بازيافت حلال…………………………………………………………………………………………………………………………………………………….65
مقدمه:
روش متداول دراستخراج فلزات متالورژي حرارتي است ولي اين روش به علل مختلف از جمله مصرف انرژي زياد وايجاد آلودگي محيط زيست امروزه در تنگنا قرار گرفته وقوانين زيست محيطي كاربرد آن را محدودتر و مشكلتر ساخته است. پيشرفت فني مهمي كه باعث افزايش استفاده از فنون هيدرومتالورژي براي استخراج مس شده كاربرد فنون استخراج با حلال است. استخراج با حلال روشي از جدا سازي است كه بر اساس توريع نابرابر يك ماده بين دو حلال غير قابل امتزاج پايه ريزي شده است .
در فرآيند استخراج مس توسط حلال,محلول آبي حاوي يونهاي مس(PLS ) وفاز آلي ((Organic كه تركيبي از استخراج كننده ورقيق كننده است با يكديگر مخلوط شده.ترجيحا يونهاي مس جذب استخراج كننده مي شوند وبه فاز آلي منتقل ميگردند.
پـس از انتقال ماده مورد نظر از مخلوط اصلي به فاز حلال بايستي دو فاز مورد نظر يعني مخلوط اصلي و حلال از يكديگـر جدا شده و هركدام براي تكميل فرآيند جداسازي به واحدهاي مربوطه انتقال يابند. استخراج كننده ماده أي با ويسكوزيته بالا است كه به شكل خالص قابل استفاده نميباشد و آن را در مايعي مناسب به نام رقيق كننده حل ميكنند. رقيق كننده استخراج كننده را در خود حل و خواص فيزيكي آن را بهبود ميبخشد. از جمله اين خواص فيزيكي ويسكوزيته، دانسيته، ثابت دي الكتريك و نقطه اشتعال است. ويسكوزيته ودانسيته فرآيند جدايش فازها را تحت تاثير قرار مي دهند . ثابت دي الكترك ميزان حلاليت تركيبات رقيق كننده را نشان ميدهند. رقيق كننده تاثير چنداني در استخراج يونهاي فلزي استخراج شونده از محلول ندارد ولي در بهبود قابليتهاي استخراج كننده از لحاظ كيفيت و راندمان استخراج از اهميت فوق العاده أي برخوردار است مهمترين خصوصيت لازم براي فاز آلي(Organic Phase) كه مجموع استخراج كننده و رقيق كننده مي باشد، غير قابل حل بودن در فاز آبي مي باشد.
1-1- تاريخچه استخراج فلزات به روش هيدرومتالورژي
استخراج اوليه مس توسط روش هاي هيدرو متالوژي تقريبا به صورت اتفاقي صورت گرفت بدين طريق كه آب ناشي از برف و باران به داخل توده هاي باطله نفوذ كرده و در چنين محيط مرطوبي با اكسيداسيون پيريت محتوي، اسيد سولفوريك و يون هاي فرو حاصل گرديد و توسط اسيد توليد شده فرايند ليچينگ مينرالهاي غير سولفيدي مس انجام و pH محلول حاصله به حد كافي جهت جلوگيري از هيدروليز مس و آهن پايين بود .
باكتريهاي موجود در توده هاي سنگ تبديل آهن فرو- فريك را تسريع كرده كه در حضور سولفات فريك مس سولفيدي نيز بصورت محلول در مي آيد در نتيجه از زير توده هاي باطله جريان از محلول با فلوي كم و محتوي مس نسبتاً بالا جاري مي شد كه مس موجود در آن در مجاورت آهن قراضه بصورت جانشيني رسوب مي نمود. بعدها در اوايل قرن بيستم استخراج مس از اين طريق تحت كنترل در آمده و قدم هاي بسيار موثري در تكميل و توسعه آن برداشته شد. امروزه روش هاي هيدرو متالوژي براي استخراج مس در مورد كاني هاي اكسيدي و باطله معادن كه مخلوطي از سولفيد و اكسيد كم عيار است اعمال مي گردند .
فنون هيدرو متالوژيكي اصولاً براي استخراج مس از كاني هاي اكسيد شده مس در كاني هاي اكسيدي كم عيار مس و باطله هاي سولفيدي به كار برده مي شود از هيدرو متالوژي همچنين در مواردي براي حل كردن متلاطم كاني هاي سولفيدي تشويه شده استفاده مي شود حدود 900000 تن مس در سال به وسيله فنون هيدرو متالوژي توليد مي شود كه 15% توليد جهاني مس از كاني ها را تشكيل مي دهد. حل كردن باطله معادن بازده بازيابي مس از كانسار را بهبود مي بخشد و اين فرايند عموميت روز افزوني پيدا مي كند علاوه بر اين مسئله خارج شدن SO2 از كارخانه هاي ذوب مس انگيزه مهمي را براي توسعه فنون هيدر متالوژي براي انجام عمليات بر روي سولفيدها به وجود آورده است. اين انگيزه منجر به توسعه و راه اندازي يك واحد پيشاهنگ براي آزمايش فرايند هاي جديد انحلال سولفيدها شده كه ممكن سرانجام به مرحله توليد صنعتي برسد .
1-2- مزايای روش هيدرو متالوژی
– خلوص فلز
عموماً، فلز بدست آمده در روش هيدرومتالوژی توسط الکتروليز يا ساير روش ها خالص تر بوده و در بسياری از حالات نياز به تصفيه بعدی ندارد
– باطله سنگ معدن
بطور کلی در فرايند هيدرو متالوژی حلال بکار برده شده روی مواد بی ارزش سنک معدن بی تاثير بوده در حالی که در روش پيرو متالوژی با اضافه کردن مواد کمک ذوب نا گزير از ذوب موادبی ارزش و تشکيل مواد بی ارزش هستيم که همراه با مصرف انرژی زياد است .
– خوردگی
بطور کلی عامل خوردگی در هيدرو متالوژی کمتر از متالوژی حرارتی است و يکی از عوامل کاهش خوردگی در روش هيدرومتالورژی کار در درجه حرارت پايين است البته در اين روش از حلال های اسيدی يا بازی استفاده می شود که مستلزم کاربرد تجهيزات مقاوم به خوردگی در برابر اسيد و باز است
- درجه حرارت پايين
– حمل و نقل مواد
جابجايي مواد در هيدرو متالوژی آسانتر و کم هزينه تر و ايمن تر است
– عيار ماده معدنی در سنگ معدن
مزيت روش هيدرو متالوژی بويژه در مورد سنگ های معدنی کم عيار آشکار می شود در اين روش فقط قسمتی از سنگ که حاوی ماده معدنی با ارزش است مورد عمل حل کردن قرار می گيرد
– نا خالصی ها
در اين روش نا خالصی های موجود در سنگ معدن در مقايسه با روش پيرومتالوژی از اهميت کمتری بر خوردار هستند . زيرا حذف نا خالصی ها از محلول آسانتر و ارزانتر از جدايش اين مواد از طريق ذوب و پالايش است
– سرمايه گذاری
سرمايه گذاری در اين روش نسبت به روش حرارتی کمتر است
– ايمنی کار
ايمنی کار در روش هيدرو متالوژی بيشتر از روش حرارتی است و علت اصلی آن ناشی از کار در درجه حرارت پايين است
– نيروی کار
در اين روش کار کار کنان در شرايط بهتر و سبک تری انجام می شود و نياز کمتری به نيروی کار است
– کاهش مصرف انرژی
– کاهش الودگی محيط زيست
خرید تحقیق کامل استخراج مس باحلال و بیولیچینگ
1-3- معايب روش هيدرو متالوژی
– عدم قابليت کاربرد روش هيدرو متالوژی برای توليد برخی عناصر
مانند سيليکاتها و غيره
– نوع حلال
بسياری از حلال های مورد استفاده در روش هيدرومتالوژی مانند آمين ها حلال های گران قيمتی هستند که کاربرد آنها باعث بالا رفتن هزينه توليد ميشود
– جدايش فاز مايع از جامد
جدايش فاز مايع از جامد در بسياری از موارد آسان نيست به عنوان مثال وجود ترکيبات رسی در سنگ معدن که در مجاورت اسيد به صورت کلوئيدی و معلق در می آيند
– با ز يابی فلزات و نوع انرژی مصرفی
در اين روش برای باز يابی فلزات از محلول از روش الکتروليز استفاده ميشود که مصرف کننده انرژی گران قيمت الکتريکی است
– آلودگی آب
– سرعت توليد
واکنش های هيدرومتالوژی به علت انجام در دمای پايين دارای سرعت کم هستند و نياز به زمان طولانی وتجهيزات با حجم زياد دارد
– کاربرد باکتری ها
در هيدرو متالوژی کاربرد باکتری برای انحلال کانی ها روز به روز توسعه بيشتری می يابد که نقش باکتری ها در سلامتی و آلودگی محيط زيست به درستی روشن نيست
– باز يابی فلزات گرانبها
حلال های مورد استفاده در اين روش فقط فلزات مورد نظر را در خود حل می کنند و چنانچه همراه اين فلزات عناصر گرانبهايی مانند طلا و نقره وجود داشته باشد باز يافت اين فلزات مقدور نيست
1-4- تاريخچه استخراج مس به روش استخراج با حلال
توليد مس به روشهاي SX/EW از قرن هجدهم آغاز شده است. تا كنون دركشورهاي آمريكاي لاتين پيشرفت هاي زيادي در اين زمينه حاصل شده است. به عنوان مثال شيلي پروژه هاي زيادي رادر اين زمينه آغاز نموده است و هنوز ادامه دارد . فرآوري مس با استفاده از حلالهاي هيدروكسي بطور عموم از 55 سال پيش آغاز شده است . مقدار زيادي از مس هاي كاتدي در در دنيا از روش ليچينگ اسيدي وسپس خالص سازي از طريق SX/EW بدست مي آيد. هزينه هاي سرمايه گذاري پايين وهزينه هاي عملياتي كم نسبت به روشهاي تغليظ ذوب وپالايشگاه وهمچنين كيفيت بالاي مس كاتدي باعث پيشرفت تكنولوژي اين روش شده است. توليد مس باعيار99/99%وهمچنين عدم وجود ناخالصي هايي از قبيل سرب ,اكسيژن , سولفور نشان از كيفيت بالاي مس كاتدي (Grade LME ) مي باشد.
كيفيت بالاي مس كاتدي تقاضاي زيادي را در بازارهاي الكترو نيكي ايجاد مي كند .
نه تنها هزينه هاي پايين روش انحلال و SX/EW بلكه آلودگي بسيار كم زيست محيطي آن از مزاياي اين روش مي باشد.روش SX/EW را بطور عام يك روش تميز مي شناسند.
آلودگي هوا وضايعات توليدي آن بسيار پايين است . علاوه بر اينها آلودگي صوتي نيز بسيار پايين است .مجموعه اي از اين عوامل باعث مي شود كه قسمتهايي از اروپا وجهان به اين روش توجه زيادي نشان دهند .
بطور كلي مزاياي روش SX/EW به قرار زير است
- استخراج انتخابي مس به عنوان يك روش شيميايي شناخته مي شود.
- محلولهاي آلي استخراج در يك سيكل بسته كار مي كنند.
- افزايش غلظت مس در محلول براي استفاده در فرآيند EWمي باشد.
- مس كاتدي توليدي كيفيت بسيار بالايي دارد.
- ميانگين هزينه توليد 40-37 سنت به ازائ هر پوند مي باشد.
مزاياي زياد روش SX/EW وهمچنين معايب بسيار پايين آن باعث انتخاب اين روش مي شود.
توليد مس به روش SX/EW اكنون در جهان بالاي 7/1 ميليون تن در سال مي باشد.
2- استخراج فلزات به روش هيدرومتالورژي
2-1-انحلال سنگ معدن
درانحلال مينرالهاي اكسيدي مس مهمترين واكنش چنين است:
كه اسيد مورد نياز اين واكنش از طريق برگشتي واحد SX/EW مي باشد .تنها راه حدر رفتن اسيد در فرآيند انحلال خاك باطله حاصل از فرآيند انحلال مي باشد.
انحلال سنگ معدن به چند روش قابل انجام است كه عبارتند از:
الف) انحلال در محل( دامپ ليچينگ)
ب) انحلال توده اي (هيپ ليچينگ)
ج)انحلال مخزني
روش انحلال به نوع و عيار مواد مورد عمل بستگي دارد . به طوركلي ، كانه هاي سولفيدي محتاج به انحلال دراز مدت هستند كه به وسيله روش هاي توده اي يا در محل مي توان به اين هدف نائل شد در حالي كه كانه هاي اسيدي را مي توان به تمام روش هاي انحلال حل كرد .
هزينه هاي سرمايه اي و بهره برداري انحلال به روش هاي توده اي ، در محل و انباشته اي پايين است و از اين رو اين روش ها براي مواد كم عيار در نظر گرفته مي شود .
پايه پدها به جهت عملياتي و يا زيست محيطي بر لاينرهاي غير قابل نفوذ استوار است. خاك در ابتدا بايستي خرد شود و دربعضي موارد آگلومره شود تا بتوان ارتفاعهاي 6 تا 7 متري خاك را مورد استفاده قرار داد.
مينرالوژي باطله ازيك معدن به معدن ديگر فرق مي كند اما مهمترين مشخصه اي كه بايد در باطله در نظر گرفته شود مقدار اتلاف اسيد مي باشد.كه اين مورد با افزايش كربناتها افزايش مي يابد.
اين مسئله ايجاب مي كند در ابتداي راه اندازي پروژه با انجام تست هايي وضعيت خاك مشخص شود. باطله ها علاوه بر اتلاف اسيد در بازيابي مس هم تاثير مي گذارند. بطور مثال افزايش مقدار كلي (خاك رس), باعث كاهش مقدار نفوذ پذيري شده يا در مواردي جريانهاي نا خواسته ايجاد مي كند.
تحقيقات اخير نشان مي دهدكه خاك رس دانه ريز به عنوان يك دزد در انحلال مطرح است كه باعث گرفتار شدن مس در هيپ مي شود.
همچنين وجود آرسنيك وكلريد در خاكهاي مس ناشي از ناخالصي هاي باطله مي باشد.
انحلال مخزني و متلاطم گرانترند و محدود به كار بر روي كاني هاي پر عيار مي شود . قبل از توسعه روش استخراج با حلال تنها روش توليد الكتروليت ، انحلال مخزني و متلاطم بوده است .
اما امروزه به كمك روش استخراج با حلال مي توان الكتروليتي از محلول رقيق حلال توليد كرد ، در نتيجه استفاده از انحلال توده اي ، انباشته اي و در محل افزايش مي يابد .
بازيابي مس از محلول هاي رقيق انحلال : سمتناسيون و استخراج توسط حلال .
محلول هاي حاوي مس از عمليات انحلال از لحاظ غلظت مس به دو دسته تقسيم مي شوند .
الف)محلول قوي حاوي g/l 50-30 مس حاصل از انحلال مخزني و متلاطم .
در اين محلول ها مقدار كافي مس براي استخراج الكتروليتي مستقيم فلز با درجه خلوص بالا وجود دارد .
ب)محلول ضعيف حاوي g/l 5-1 مس حاصل از انحلال در محل ،توده اي و انباشته اي مقدار مس اين محلول براي استخراج مستقيم الكتروليتي كافي نيست
هر دو نوع محلول حاوي ناخالصيهاي موجود در كانه از قبيل آهن و ساير فلزات مثل كادميم ، سرب و روي هستند .
محلول هاي حاوي g/l 50- 30 مس پيش از استخراج الكتروليتي فقط بايد خالص شوند . به طور كلي براي رسيدن به اين هدف آهن سه ظرفيتي را از محلول هوا دهي شده با آهك زنده ، با pH حدود 3 الي 5/3 رسوب مي دهند و به آرامي از مدار خارج مي كنند .
روش ديگر جدا كردن بخشي از محلول از مدار و مس زدايي آن است با پيدايش حلال هاي جديد (استخراج كننده ها) براي استخراج مس از محلول هاي اسيدي مي توان جانشيني براي فرايند سمتناسيون به دست آورد اين حلال ها (به ويژه واكنش گرهاي ليكس Lix از شركت جنرال ميلز كميكا لز و واكنشگرهاي كلكس Kelex از شركت اشلند كميكالز)اين امكان را مي دهند.
الف) مس از محلول رقيق توسط حلال استخراج و وارد فاز آلي شود
ب) الكتروليت هاي غليظ از مس مناسب براي استخراج الكتروليتي توليد شوند.
الكترليت ها به وسيله اين فاز آلي محتوي مس با محلول سولفوريك اسيد به دست مي آيند.
2-1-1- روشهاي انحلال سنگ معدن :
عمل استخراج از جامد عبارت است از حل شدن انتخابي يك يا چند جز از يك مخلوط جامد در تماس با يك محلول مايع ، اين فرايند يكي از قديمي ترين عمليات واحد در صنايع شيميايي است كه با توجه به روش كار اسامي مختلفي به آن اطلاق مي شود . مفهوم استخراج از جامد از نفوذ مايع به درون بستر ثابتي از جامدات ريشه مي گيرد ولي امروزه معاني مختلفي براي بيان اين عمليات به كار مي رود .
صنايع فلز شناسي شايد بيشترين استفاده كننده عمليات استخراج جامد باشد . بيشتر مواد معدني با ارزش به نسبت زيادي با اجزاي ناخاسته اي مخلوط مي باشند كه روش استخراج از جامد براي جدا سازي اجزا با ارزش مناسب مي باشد . براي مثال ، مس توسط استخراج با اسيد سولفوريك از بقيه مواد موجود در سنگ معدن جدا مي شود .
– آماده سازي جامد:
چگونگي عمل استخراج از جامد و روش به كار رفته تا حد زيادي به عملي كه قبلاً روي جامد انجام شده بستگي دارد . در بعضي مواقع ، ذرات كوچك ماده حل شونده كاملا توسط يك جسم نا محلول احاطه شده است . بنابراين حلال بايد در جسم مربوطه نفوذ كرده و محلول حاصل نيز بايد قبل از جدا سازي ، به بيرون نفوذ كرده اين وضعيتي است كه صنايع فلزي در بسياري موارد با آن روبرو هستند . خرد كردن و آسياب كردن چنين جامداتي عمل استخراج را به ميزان قابل توجهي تسريع مي كند .
براي مثال ، سنگ معدن مس را مي توان توسط محلول اسيد سولفوريك و با عبور دادن خاك مربوطه از غربال MESH 60 ظرف 4تا 8 ساعت استخراج نمود .
اگر به صورت دانه هاي 6mm باشند 5 روز طول مي كشد و اگر كلوخه هاي 150mm به كار روند 4 تا 6 سال زمان لازم است. از آنجاييكه آسياب كردن پر هزينه است . اندازه ذرات را از روي درجه مرغوبيت و ارزش سنگ معدن انتخاب مي كنند .
عمليات استخراج ازجامد تحت شرايط نيمه پيوسته (ناپايدار) وهمچنين تحت شرايط كاملا مداوم وجود دارد. دو روش اصلي مماس وجود دارد : يكي پاشيدن يا چكيدن مايع روي جامد ، ديگري فرو بردن جامد بطور كامل در مايع.
انتخاب نوع دستگاه در هر صورت بستگي به حالت فيزيكي جامد و مشكلات و هزينه حمل و نقل آن دارد.
استخراج از جامدات بصورت توده اي :
سنگ هايي كه درصد ماده معدني مطلوب در آنها كم است و ارزش خرد و آسياب كردن ندارند روي سطح زمين نفوذ ناپذير به صورت توده ای از کلوخه هايی که از معدن در آورده شده جمع می کنند . مايع استخراج کنننده را روی سنگ معدن ريخته و بعد از اينکه از توده خارج شد جمع آوری می کنند.
- واحد انحلال توده ای(HEAP LEACHING) در مس سرچشمه
خاك حمل شده به هيپ عمدتا از کانی های مسی می باشد که قسمت اعظم آن از کانی های اکسيدی و قابل حل به وسيله اسيد سولفوريک رقيق می باشد. عمليات انحلال در هيپ در يک سيکل بسته انجام می شود. در کارخانه ليچينگ در واحد استخراج با حلال (SX) به کمک يک ماده آلی يون های مس از محلول خروجی از واحد انحلال توده ايی جدا می گردد سپس رافينيت خروجی از واحد استخراج با حلال که ترکيبی از اسيد سولفوريک و آب و غلظت پايينی از مس می باشد.
به وسيله پمپ های گريز از مرکز به واحد انحلال توده ای برای پاشش ارسال می گرد. محلول پاشيده شده بر روی هيپ از ميان کانسنگ می گذرد . مس و ساير عناصر قابل حل از جمله آهن را شسته و در سطح قاعده هيپ جمع می کند و از آنجا به داخل حوضچه جمع کننده محلول باردار يونی منتقل می سازد . محلول جمع آوری شده در داخل پوند به مسئله پمپ های گريز از مرکز به واحد هيپ برای پاشش فرستاده می شود .
2-2-1- هيپ و سيستم جمع آوری زيرهيپ :
هيپ از دو ناحيه شرقی و غربی تشکيل شده است اين دو ناحيه از لحاظ ساختمانی و شکل توپر گرافی تقريبا شبيه می باشند. يک آستر (liner) از جنس پلی اتيلن (HDPE) به ضخامت 1mm و با مساحت 230000 متر مربع بين دو لايه محافظ رسی به ضخامت 20cm جهت فرآهم نمودن سطح نفوذ ناپذير قرار گرفته است. روی لايه محافظ رسی بالای لاينر پنج عدد لوله به قطر 400mm و يک لوله به قطر 315mm از جنس پلی اتيلن قرار گرفته است که وظيفه اين لوله ها انحلال محلول جمع شده در سطح قاعده هيپ به حوضچه جمع کننده محلول باردار يونی می باشد . روی اين لوله های جمع کننده و در کل قاعده هيپ گراول به ضخامت40cm ريخته شده است و برای جلوگيری از رانش لايه رسی روی گراول يک لايه خاک اکسيدی به ضخامت 1m در کل هيپ ريخته شده است . کل منطقه هيپ از 16 ناحيه (پداگ) تشکيل گرديده است که نواحی زوج به تعداد 8 عدد در دره غربی و به تعداد8 عد در دره شرقی قرار گرفته اند . ارتفاع هر ناحيه4/33m و سطح هر ناحيه حدود10200m2 می باشد. به طور متوسط 9800 تن خاک اکسيدی با دانسيته 1/52 ton/m3در روز توسط کاميون روی نواحی واحد انحلال توده ای ريخته می شود که سيکل خاکريزی هر ناحيه حدود 7/5 روز به طول می انجامد . بعد از اتمام خاکريزی و آماده سازی سطح ناحيه 5/3 روزاميتر گذاری ناحيه زمان می برد . شپش خيساندن ناحيه به مدت 7 روز و تحت پاشش بودن ناحيه 60 روز زمان می برد و در نهايت بعد از اتمام سيکل پاشش برای لوله برداری ناحيه زمانی برابر 5 روز در نظر گرفته شده است.لذا از زمان شروع خاکريزی تا زمان لوله برداری مجموعا 83 روز طول می کشد و بعداز لوله برداری مجددا سيکل خاک برداری آغاز می گردد.
2-2-3- هيپ و سيستم پاشش روی هيپ:
محلول باردار يونی خروجی از هيپ پس از ارسال به واحد استخراج و از دست دادن مس و جبران نمودن اسيد آن مجددا به هيپ ارسال می گردد . رافينيت به ظرفيت 2400 متر مکعب می شود . سپس اين محلول به وسيله دو عدد پمپ در حال کار و يکی در حال استراحت به داخل حلقه اصلی دور هپپ پمپ می گردد . برای هر ناحيه (پداگ) یک انشعاب از حلقه اصلی (ring main ) گرفته شده است اين انشعاب به يک شير فشار شکن روی ناحيه وصل می گردد و بعد از شير فشار شکن لوله های ساب ماين (sub main ) قرار گرفته اند . روی اين لوله ها به فاصله m 762 % انشعاباتي به نام اميترگرفته شده است که روی اميترهای فوق قطره چکان به فاصله m 762 % از يکديگر قرار دارد. ميزان دبی هر قطره چکان بطور نرمال بايستی 2/7 لیتر بر ساعت در هر متر مربع باشد . رافينيت پاشش با غلظت 35 % گرم بر ليتر مس و 30 گرم بر ليتر اسيد بر روی هيپ پاشيده می شود و غلظت محلول باردار يونی خروجی از واحد انحلال توده ای 5/3 گرم بر ليتر مس می باشد .
محلول باردار يونی PLS (pregnant leach solution ) خروجی از زير واحد انحلال توده ای وارد پوند PLS به ظرفيت 14400 متر مکعب گرديده و سپس محلول توسط 3 عدد پمپ پس از عبور از تانکهای فشار شکن به سمت واحد استخراج با حلال ارسال می گردد.
ضمن اينکه پوند storm (ذخيره) به ظرفيت 7350 متر مکعب جهت جمع آوری آبهای سطحی و جمع آوری محلول حاصل از سر ريز شدن پوند PLS در نظر گرفته شده است .
2- فرآيند استخراج با حلال : (Solvent Extraction )
روشهاي استخراجي بيش از 55 سال است كه در پالايشگاهها مورد استفاده قرار مي گيرد. اين روش در صنايع متالورژيكي از سال 1960 به كار رفته است . اين روش از دهه هاي 40 و50 براي انرژي اتمي به كار رفته است. مقدار زيادي ارانيم مورد مصرف در نيروگاههاي هسته اي به روش SX تهيه شده است. همچنين تعدادي از عناصر مثل پلوتونيم Amercium ,Corium و… توسط تكنيكهاي SX خالص گرديده اند.در حال حاضر روش SX جهت بازيابي ارانيم ,واناديم ,تنگستن ,توريم وبر متداول است. همچنين بازيابي تانتاليم,كلمبيم,زيركونيم,كبالتوفلزاتنادر از اين طريق امكانپذير مي باشد . مقداز زيادي فلزات مس ,نيكل روي به اين روش استحصال مي گردد.
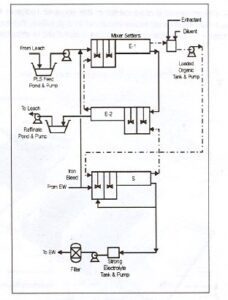
شكل شماره (1) مدار فرآيند ليچينگ
– استخراج با حلال در مورد مس شامل مراحل زير است :
الف)استخراج انتخابي مس از محلول اسيدي حاصل از انحلال و بردن آن به فاز آلي نامحلول .
ب)جدا كردن مس از فاز آلي و بردن آن به داخل محلول اسيدي غليظ (g/l 185-150سولفوريك اسيد)اين محلول مقدار زيادي مس را جذب مي كند و الكتروليتي مناسب براي استخراج الكتروليتي است حلال آلي ناخالصي ها را در خود حل نمي كند به طوري كه آن ها را در محلول اوليه حاصل از انحلال باقي مي مانند . بنابراين الكتروليت نهايي عاري از هر گونه ناخالص است .
– محاسن استخراج از روش حلال عبارتند از :
الف)الكتروليتي با غلظت كافي مس جهت استخراج الكتروليتي ، مستقيما از محلول رقيق حاصل از انحلال به دست مي آيد
ب)ناخالصي هاي محلول حاصل از انحلال وارد الكتروليت نمي شوند
هر دوي اين امتيازها براي كار بر روي محلول رقيق مس مهم هستند و امتياز (ب) ممكن است در فرايند توليد الكتروليت خالص از محلول غليظ حاصل از انحلال (g/l 30 مس )كه به وسيله هارت لاژ Hartlage و كورن برگ Cornberg پيشنهاد شده به كار گرفته شود .
2-1- شيمي فرآيند استخراج با حلال :
مهم ترين حلالهاي آلي براي استخراج مس از محلول هاي حاصل از انحلال عبارتند از معرف هاي ايكس و معرف هاي كلكس كه هر دوي آنها عامل هاي كي ليت ساز هستند . حلالها اغلب در يك ماده حامل آلي ( به عنوان مثال نفت ، 5 تا 20 در صد حجمي) به منظور به دست آوردن مايعي با ويسكوزيته كم حل مي شوند .
دونوع عمليات SX وجود دارد , اولي تبادل يوني مايع –مايع است كه در اين روش جزء كوچكي از يك ماده آلي شيميايي(استخراج كننده ) در مايع آلي دومي به نام رقيق كننده حل مي گردد. رقيق كننده موادي از قبيل مشتقات نفتي يا هيدروكربنها مي باشد. در حين عمليات استخراج جزء فعال با يونهاي آبي خوراك واكنش داده وماده جديدي حاصل مي شود. نوع دوم SX تمام فاز آلي به عنوان حلال به كار مي رود , به طوري كه فاز آلي با يك يا چند جزء فاز آبي واكنش مي دهد . به عنوان مثال عمليات يدزدايي نمونه اي از اين نوع SX مي باشد. در حالت اول يك يون با جزء فعال واكنش داده وملكول كمپلكس حاصل مي گردد, در حالت دوم يك ملكول خنثي خاصيت حل كننده گي پيدا مي كند . هدف ما در اينجا بر روي تبادل يوني مس متمركز مي گردد.
عملياتي كه در فرآيندهاي انحلال , استخراج باحلال وEW انجام مي شود به صورت سه چرخه محلول بسته عمل مي نمايد. مانند شكل شماره ( 1 ). چرخه اول مس موجود در محلول حاصل از فرآيند انحلال جذب ملكول استخراج كننده موجود در فاز آلي مي شود وتشكيل فاز آلي اشباع از مس ( Loaded Organic ) را مي دهد. چرخه دوم واحدSX را نشان مي دهد . محلول ارگانيك باردار در تماس با الكتروليت قرار گرفته و مس محتوي خود را به الكتروليت پس مي دهد وآن را به الكتروليت قوي تبديل مي نمايد . در نهايت چرخه سوم قرار داردكه الكتروليت قوي به واحد EW منتقل ميشود وپس از آنكه مس آن جذب ورقه هاي كاتد شد مجددا به واحد SX منتقل ميگردد.
مس كاتدي با خلوص بالا روي ورقه هاي كاتد اوليه رسوب مي نمايد .
روشهاي استخراج با حلال جهت جداسازي يك جزئ به طور انتخابي از بقيه اجزائ موجود در محلول آبي مورد استفاده قرا ر مي گيرد.
در فرآيند ليجينگ محلول حاصل از انحلال شامل اجزائي از قبيل , CU 2+ Fe 2+ , Fe 3+, Zn2+ Ca2+ , Mn2+ , Mg2+ , Al3+ , Mo 6+ و…كه همگي از خانواده سولفاتها بوده مي باشند.
استخراج مس از محلول PLS با استفاده از فاز آلي يك واكنش تبادل يوني است
در فرآيند استخراج مس با حلال يونهاي مس از محلول PLS درنهايت به واحد EW منتقل مي شود.همچنين يونهاي هيدروژن در جهت عكس يونهاي مس منتقل خواهند شد.
انتقال يونهاي مس به فاز آلي يك واكنش دو طرفه بوده كه توسط غلظت اسيد محلول آبي كنترل مي گردد. در واحد استخراج پايين بودن نسبي غلظت اسيد (g/l 5-4) در محلول PLS اين اجازه را مي دهد كه يونهاي مس با يونهاي هيدروژن موجود در فاز ألي جابجا شوند. كه در اثر اين فرأيند عمل استخراج مس انجام شده ودر ضمن غلظت اسيد در فاز آلي افزايش مسي يابد.
محلول آبي فقير از مس (Raffinat ) بهمراه ساير ناخالصيهاي باقيمانده در آن دوباره به پدهاي واحد انحلال منتقل مي گردد.
در واحد عريان سازي (Stripping ) واكنش عكس در حين تماس فاز آلي باردار با محلول الكتروليت كه تقريبا g/l180 اسيد دارد , انجام مي شود . در اين مرحله فاز آلي اشباع از مس با التروليت ضعيف برگشتي از واحد EW مخلوط مي شودويونهاي هيدروژن درفاز اب الكتروليت با يونهاي مس در فاز ألي جابجا مي شوند وغلظت مس در الكتروليت افزايش مي يابد. فاز ألي خروجي از واحد عر يان سازي مجددا به واحد استخر اج منتقل مي شود ومورد استفاده قرار مي گيرد.
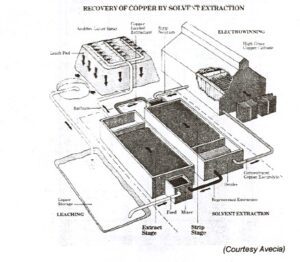
شكل شماره (3 ) شماتيك فرآيند استخراج
به طور كلي استفاده ازنوعي استخراج كننده كليت كننده در تبادل يوني مس, مهمترين موفقيت در بازيابي مس از محلولهاي حاصل از انحلال مي باشد. انواع مختلف ملكولهاي استخراج كننده با بار خنثي يا باردار وجود دارد .وجود يونهاي هيدروژن با بار صفر يا بار مثبت نشان دهنده رفتار ملكول كليت كننده مي باشد,كه در حين فرآيند تشكيل حلقه اي شامل يون فلز وملكول استخراج كننده را مي دهد. اولين روش استخراج مس به روش هيدرو بصورت فرآيند دامپ ليچينگ بوده است.تا قبل از آن تنها مس به روش سمنتاسيون از محلول باز يابي مي شده است.محصول حاصل از اين روش مشكلات بعدي از قبيل ذوب وپالايش را به دنبال داشت. درصنعت جهت كاهش سرمايه گذاري وحذف بخشي از تجهيزات وكاهش ميزان اسيد مصرفي شرايطي ايجاب نمود كه مواد شيميايي ساليسيلات اكسيم جهت بازيابي مس از محلولهاي آبي مورد استفاده قرار گيرد.مطالعات وتحقيقات جهت بالا بردن قابليت اين مواد كليت كننده جهت جذب يونهاي مس و بهبود شرايط جدايش فاز وقدرت انتخابي همچنين افزايش سرعت واكنش اين تركيبات انجام شده و در حال انجام است. بطور كلي كيفيت اين مواد شيميايي بايد افزايش يابد.سرعت سينتيكي مواد جديد اين معني را مي دهد كه يك كارخانه با دو مرحله استخراج ويك مرحل استريپينگ مي تواند بجاي كارخانه اي با سه مرحله استخراج ودو مرحله استريپينگ به كار رود. PH پايينتر از 5/1 باعث كاهش سريع ظرفيت مس گيري مي شود بطوريكه در PH حدود 5/0 اين ظرفيت يك پنجم PH برابر5/1 مي باشد.
PH در محلولPLS اوليه بايد به قدري بالا باشد تا امكان بكار گرفتن در صد بالاي استخراج كننده را داشته باشد بطوري كه بتوان مس محتوي كه بالاي g/l 30 را استحصال نمود.
در شرايط نرمال كه محلولهاي انحلال بين 2 تا g/l 3 مس دارند PH بايد بين 2 تا 5/2 باشد.هر يك درصد حجمي غلظت استخراج كننده موجود در فاز ألي حد اقل g/l 25/0 از مس محلول PLS را در شرايطي كه نسبت O/A ( 1:1) باشد پوشش ميدهد.
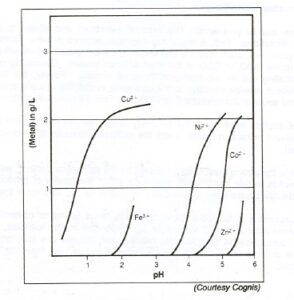
شكل شماره (4) مشاهده خاصيت انتخابي استخراج كننده
همانطوري كه در شكل شماره (4) مشاهده مي شود خاصيت انتخابي ماده كليت كننده براي مس در مقايسه با ساير فلزات بالا مي باشد. البته تنها يون فلزي كه مي توان در اين مورد در نظر گرفت كه رفتار آن نزديك به يونهاي مس مي باشد يونهاي آهن فريك مي باشند.
2-2- سينتيك فرآيند استخراج باحلال :
بعضي از عوامل از اهميتي معادل اهميت توزيع تعادلي مس بين فاز آلي و فاز آبي برخوردارند
الف)آهنگ نيل به شرايط تعادل
ب)آهنگ رهايي فاز آلي و فاز آبي از امولسيوني كه در خلال سه مرحله تماس (مخلوط شدن)ايجاد مي شود . مواد حامل و تنظيم كننده هاي فاز آلي بطور موثري بر اين آهنگ ها تاثير مي گذارند.
در مقياس آزمايشگاهي بعد از 2-1 دقيقه اختلاط آلي-آبي شرايط تعادل حاصل مي شود .
سيستم هاي صنعتي به نحوي طراحي شده اند كه 4-3 دقيقه از زمان صرف هم زدن شود و آهنگ نيل به تعادل بر اثر افزايش دماي محلول ها وبا استفاده ازمواد حامل حاوي اندكي تركيبات معطرافزايش مييابد .آهنگ رهايي فاز آلي و آبي عامل مهمي در طراحي ها به حساب مي آيد زيرا اين آهنگ بر سطح ته نشين ساز و زمان ته نشين شدن تاثير مي گذارد.
3- مواد مصرفي درفرآيند استخراج باحلال (SOLVENT EXTRACTION ) :
عمده مواد مصرفي در فرآيند استخراج با حلال اجزاء تشكيل دهنده فاز آلي يعني رقيق كننده ها واستخراج كننده ها مي باشند.
3-1- استخراج كننده هاي مصرفي در فرايند استخراج باحلال:
3-1-1- خصوصيات يك استخراج كننده مطلوب در فرايند استخراج باحلال:
- ارزان و در دسترس باشد
- حلاليت خيلي كمي در فاز آبي داشته باشد
- پايداري خوبي داشته باشد . يعني اينكه بتواند مدتها در يك حلال عمل فراوري را انجام دهد, بدون اينكه فاسد شود.
- در فاز آبي درهنگام آميزش, پراكندگي (Emulsion) ايجاد نكند.
- زماني كه با يك رقيق كننده (Diluent)آميخته مي شود, ويژگي لخته سازي(Coalescing ) مناسبي داشته باشد.
- قابليت بارگيري فلزات سنگين را داشته باشد.
خرید تحقیق کامل استخراج مس باحلال و بیولیچینگ
3-1-2-شيمي تجزيه اكسيم در واحدهاي استخراج با حلال ( SX ) :
اكسيمها به عنوان استخراج كننده در فرآيندهاي استخراج با حلال استفاده مي شوند و تحت شرايط نرمال عملياتي فعاليت آنها بتدريج كاهش مي يابد. واكنش هاي تجزيه شامل هر دو گروه اكسيمين و حلقه آروماتيك مي شود : هيدروليز آكيسمها يك آلدئيد يا يك كتون توليد مي كند كه در فاز آلي جمع مي شوند و باعث مي شود شرايط جدايش فازها بدتر شود. نيتراسيون حلقه آروماتيك واكنشي تجزيه مهمي است كه با حمله ( برخورد ) يك يون نيترونيم الكترفيليك با اتم اكسيژن ( O ) حلقه فنليك اتفاق مي افتد . وجود يونهاي نيترات باعث افزايش تجزيه و توليد محصولات كربونيليك بطور جزئي د رمدار استريپينگ مي شود . الكلها توسط تري دكانول و P – نونيل فنل تهييج ( برانگيخته ) مي شوند و باعث تشكيل اكسازول در فرآيند تجزيه فتوشيمي مي شوند . سولفوناسيون حلقه آروماتيك اغلب توسط تماس تصادفي بين فاز آلي و اسيد سولفوريك غليظ صورت مي گيرد. شواهد آزمايشگاهي نشان مي دهد كه اصلاح كننده هاي تعادلي تاثير مهمي روي پايداري اكسيمها دارند . محصولات تجزيه كه مشخصات پلار ( قطبي ) دارند شرايط تجزيه فاز را در فرآيند بوجود آورده و سرعت تجزيه را شتاب مي دهند اين امر به اين دليل است كه سطح مايع – مايع را افزايش مي دهد . بعد از سال 1963 زمانيكه آسيابهاي عمومي معرفي شدند ، LIX 63 و LIX 64 N و بسياري هيدروكسيمهاي پايه استخراج كننده ها براي فرآيندهاي براي استخراج با حلال بصورت تجاري معرفي شده اند . جزء فعال در LIX 63 ، 5 ، 8 دي اتيل – 7 – هيدروكسي – 6 – 2 دكانون – اكسيم مي باشد كه يك اكسيم آليفاتيك ضعيف است و اين ماده بطور اقتصادي مس را از محلولهاي دامپ ليچينگ استخراج مي كند ( 1 ) . يك گروه ديگر استخراج كننده ها LIX 64 N است كه يك اكسيم آرماتيك مي باشد كه توسط افزودن 2 – هيدروكسي – 5 – دودسي بنزوفنون اكسيم به LIX 63 توليد مي شود كه مانند بقيه استخراج كننده ها قابليت استخراج مس را دارد .
بطور كلي 3 تركيب فعال در استخراج كننده هاي مس وجود دارد كه عبارتند از :
- 2 –هيدروكسي – 5 – نونيل بنزو فنون اكسيم .
- هيدروكسي – نونين بنزآلدئيد اكسيم .
- 2 – هيدروكسي – 5 – دو دسي بنزآلدئيد اكسيم .
شركتهاي كوگنيس ( Cognis ) و اوسيا ( Avecia ) فقط 2 توليد كننده مهم اين مواد هستند .
استخراج كننده هاي تجاري با يكديگر رقابت مي كنند و نيمي از كيفيت آنها مربوط به شركت تهيه كننده مي باشد .تلفات اكسيم در واحدهاي SX بصورت ماندگي فازي ( Entraiment ) بوجود مي آيد ، ميزان تجزيه و حلاليت پارامترهاي مهمي هستند كه در ميزان تلفات نقش دارند.
واكنش اصلي تجزيه اكسيمهاي هيدروليز شدن مي باشد كه توسط تماس بين فاز آلي و الكتروليت كه معمولاً 180 تا 220 گرم بر ليتر اسيد سولفوريك دارد بوجود مي آيد ، محصولات واكنش آلدئيدها و كتونها هستند . با توجه به نوع اكسيم يك آلدوكسيم يا يك كتوكسيم توليد مي شود .
ديگر واكنشهاي تجزيه ، نيتراسيون ، فتواكسيداسيون ، الكلي شدن ، دي هيدراته شدن و سولفوناته شدن مي باشد . پايداري اكسيمها با توجه به هيدروليز و نيتراسيون اغلب بصورت آلدوكسيم > > كتوكسيم است. رقيق كننده ها از تجزيه و كاهش فعاليت رنج مي برند . مهمترين حالت تجزيه ميكروبيولوژي است . باكتريها شاخه هاي كربن را از اجزاء آليفاتيك رقيق كننده جدا مي كنند اما قادر نيستند از حلقه هاي آروماتيك جدا كنند . آلكانهاي كوتاه ، الكلها ، آلدئيدها و كربوكسيليكها كاملاً خودشان پايدارند و مي توانند به ميزان زيادي روي پايداري اكسيمها تاثير بگذارند .
3-1-2-1- تجزيه اكسيمها :
الف- هيدروليز اكسيمها :
هيدروليز اكسيمها اغلب مهمترين واكنش تجزيه در واحدهاي SX است كه آلدئيدها يا كتونها را توليد مي كند . مكانيزم توليد آلدوكسيمها و كتوكسيمها در شكل شماره ( 5 ) نشان داده شده است .
با افزايش غلظت اسيد ، درجه حرارت و كشش بين مولكولي بالا شرايط تجزيه مناسب فراهم مي شود . كشش سطحي تمايل بين دو فاز را افزايش مي دهد.
در نتيجه تجزيه هيدوركسي لامين فاز آلي را ترك مي كند و بدليل خاصيت قطبي و حلاليت در آب وارد فاز آبي مي شود ، به اين ترتيب واكنش در جهتي پيش مي رود كه باعث تجزيه اكسيم مي شود . مطالعات سيستماتيك روي تجزيه هيدروليتيك اكسيمها در منابع 3 ، 8 ، 9 و 10 آمده است .در شرايط نرمال پذيرفته شده كه پايداري كتوكسيم بيشتر از آلدوكسيم است اين امر در شكل شماره ( 6 ) نشان داده شده است . همچنين دو دسي آلدوكسيم اغلب پايدارتر از نونيل آلدوكسيم است .از نظر پايداري تركيبات بصورت زير مي باشد :
آلدوكسيم > كتوكسيم > آليفاتيك اكسيم > بنزوفنون اكسيم
درمقايسه باآلدوكسيمها كتوكسيم وبنزوفنون اكسيم دو شاخص نامناسب براي هيدروليز دارند:
- گروه متيل يافنيل كه با كربن اكسيم پيوندداردخاصيت الكتروفيليك راكاهش مي دهد
- براي يك بنيان هسته دوست يك ممانعت فضائي وجود دارد مثل گروههاي متيل و فنيل كه با هيدروژن آلدوكسيمها مواجه مي شود .كتوكسيمها براي استريپ مس نياز به اسيديته پائين تري دارند و در فرآيندهاي صنعتي شرايط بحراني كمتري ايجاد مي كنند .
شكل شماره ( 6 ) تجزيه 2- هيدروكسي – 5 – نونيل استوفنون اكسيم K9 ومخلوط 2- هيدروكسي- 4- نونيل بنزآلدئيداكسيم C9 + K9 . همان غلظت كل مولي اكسيم.
تست هاي در مقياس كوچك (Batch)با 35% حجمي استخراج كننده , الكلروليت آبي با غلظت g/l 500 اسيد سولفوريك , نسبت حجمي 1 : 1 ,دماي C 45 , رقيق كننده Escaid 100 , مدت آزمايش 10 روز بوده است.تجزيه هيدروليتيك به شدت وابسته به غلظت اسيد است كه در شكل شماره (7) تاثير افزايش غلظت اسيد از 300 به g/l 500 نشان داده شده است.
(Batch)با 35% حجمي استخراج كننده , الكتروليت آبي با غلظت 300و g/l 500 اسيد سولفوريك , نسبت حجمي 1 : 1 ,دماي C 45 , رقيق كننده Escaid 100 , مدت آزمايش 10 روز بوده است.
به عبارت ديگر اصلاح كننده ها همچون تري دكانول و نونيل فنل تجزيه هيدروليتيك اكسيمها را در محيط نيترات و سولفات افزايش مي دهند . ( 6 و 3 ) كتوكسيمها كمترتحت تاثير حضور اصلاح كننده ها قرار مي گيرند . شكل شماره ( 8 ) نشان مي دهد تاثير افزايش % 10 تري دكانول به يك آلدوكسيم را روي سرعت تجزيه نشان مي دهد . از يك نقطه نظر مشكل الكلي شدن اتفاق مي افتد . زيرا شاخه آلكيل الكل با شكست باند اكسيژن آن تشكيل يك كربنات مي دهد كه خيلي ناپايدار است و بطور تناوبي الكل ممكن است افزايش يابد . خاصيت الكتروفيليك گروه اكسيمين بخاطر باند هيدروژن است بطوريكه اتم اكسيژن در گروه كربنيل از آب مي باشد و نه از خود الكل .
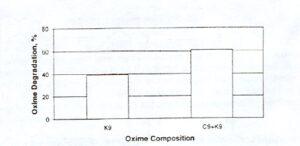
شكل شماره ( 8 ) تجزيه 2- هيدروكسي – 5 – نونيل بنزآلدئيداكسيم.
تست ها در مقياس كوچك (Batch)با 35% حجمي استخراج كننده , الكتروليت آبي با غلظت 3 g/l 500 اسيد سولفوريك , نسبت حجمي 1 : 1 ,دماي C 45 , رقيق كننده Escaid 100 , مدت آزمايش 10 روز بوده است.بطور مستقل مكانيزم مشخص يك موضوع واقعي است كه الكلها تجزيه اكسيمها را افزايش مي دهند و آلدائيد يا كتون در ساختار فاز آلي توليد مي كنند . از نظر فيزيكي آلدائيد و كتون كاملاً مشابه با اكسيم هستند . بنابراين بعد از تنظيم غلظت اكسيم اوليه ويسكوزيته و دانسيته افزايش مي يابد و رفتار فاز آلي بصورتي است كه غلظت استخراج كننده بالاتر مي رود .
انتقال مس ممكن است تحت تاثير قرار بگيرد . آلدائيدها و كتونها اصلاح كننده هاي اكسيمي ضعيف هستند .
ب- نيتراسيون :
نيتراسيون اكسيمها يك واكنش جانشيني الكتروفيليك است كه در يك شرايط مشخصي در فرآيندهاي صنعتي انجام مي شود . وقتي غلظت نيترات در PLS بالاتر از 5 تا 10 گرم بر ليتر و PH زير 1.5 باشد اتفاق مي افتد . شواهد نشان داده است كه نيتراسيون اكسيمها در غلظت نيترات حدود PPM 200 و غلظت اسيد 200 گرم بر ليتر در محلولهاي الكتروليت EW انجام مي شود . مكانيزم نيتراسيون نياز به وجود يون نيترونيوم بر اساس معادلات 1 و 2 دارد .
NO3ˉ + H2SO4 HNO3 + HSO4ˉ
HNO3 + H2SO4 NO2+ + H2O + HSO4ˉ
كنترل مقادير نيتراسيون اكسيم بر اساس غلظت نيترات ، غلظت اسيد ، كشش سطحي ، پتانسيل شيميائي و فعاليت ديگر اعضاء در فاز آلي و آبي مي باشد .
در طي سال 1999, مينر لوموس باياس از كشور شيلي شدت نيتراسيون آلدوكسيم را در فاز آلي مطالعه كرد.غلظت نيترات محلول pls 34-28 گرم بر ليتر وPH محلول 2-8/1 بود.
غلظت نيترات در الكتروليت ppm 200-40 وغلظت اسيد الكتروليت 170-160 گرم بر ليتر بوده است.
ميزان پيشرفت واكنش تواما وابسته به غلظت اسيد ونيترات مي باشد. در حدود 80% نيتراسيون در واحد استخراج و20% در واحد استريپينگ تخمين زده شده است.
مخلوطهاي آلدوكسيم – كتوكسيم كار نشده فقط توسط 100% كتوكسم عمليات صورت گرفته است.
پايداري اكسيمها در مقابل نيتراسيون در واحدهاي SX اغلب بصورت زير طبقه بندي مي شود :
نونيل آلدوكسيم > دو دسيل آلدوكسيم >> نونيل كتوكسيم
اين مطلب يك قانون عمومي نيست بلكه وابسته به نوع مخلوط استخراج كننده هاي تجاري و همچنين تركيب PLS و الكتروليت مي باشد .
بر طبق معادله (1) غلظت اسيد نيتريك مولكولي قدرت يون نيترونيوم را تعيين مي كند . غلظت اسيد نيتريك مولكولي وابسته به غلظت و غلظت اسيد سولفوريك آزاد است . حسن بسيار بالا براي سيستم HNO3 / NO3ˉ توسط رابطه زير مشخص مي شود .
كه e شرايط تعادلي را نشان مي دهد . بالانس جرم براي واكنش بايستي برقرار شود :
[ NO3 ˉ ] e +[ HNO3 ] e = [ NO3 ˉ ] t
[ NO3 ˉ ] t ، غلظت كل يون نيترات در PLS يا الكتروليت مي باشد . از تركيب دو معادله فوق غلظت HNO3 براي نيتراسيون محاسبه مي شود :
شكل شماره (10) غلظت [ HNO3 ] e براي نيتراسيون در فرآيندهاي استخراج و استريپينگ مشخص مي كند .
با توجه به موارد فوق الكتروليتي با غلظت 180 گرم بر ليتر اسيد سولفوريك و 150 PPM ، NO3 ˉ معادل با محلول PLS است كه 6 گرم بر ليتر NO3 ˉ و PH برابر با 8/1 مي باشد .
توصيه عملي اين است كه غلظت نيترات در الكتروليت زير 100 PPM و ترجيحاً زير
50 PPM باشد .
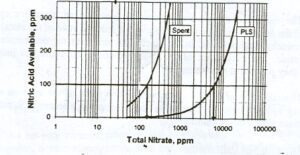
شكل شماره (10) توانائي اسيد نيتريك مولكولي براي نيتراسيون در PLS و محلول الكتروليت بصورت تئوري :
يك تاثير تحريك كننده احتمالي NO + در گسستن پيوند دوگانه كربن ، نيتروژن مي باشد كه مشابه با تاثير يونهاي NO2 + در هيدروليز اكسيمها مي باشد ، اين امر تجزيه اكسيم را به آلدائيد و كتونها در حضور غلظت پائين نيترات و غلظت بالاي اسيد نشان مي دهد . نيتراسيون جانشين شدن فنلها در حضور نيتراتهاي فلزي سنگين همچون (III ) Fe و ( II ) Cu ( 23 و 22 ) ، كه هميشه در الكتروليتهاي صنعتي مس وجود دارد ، بايستي توجه شود كه آهن باشد در حالت اكسيد شده باشد تا شرايط تجزيه در پتانسلهاي اكسايش بالا مناسب مي شود ، بنابراين پتانسيل پيشنهادي پتانسيل اكسايش ملايمي در الكتروليت است كه زير 600 MV/Sec مي باشد .
امروزه اكثر واحدهاي SX سطح دنيا بطور پريوديك از كلي هاي فعال شده براي تميز نمودن فاز آلي استفاده مي كنند ، اين ممكن است در پايداري استخراج كننده ها مناسب باشد زيرا سليكاژل و كلي ها مثل مونت موريلونيت در فاز آلي ممكن است نيتراسيون برخي تركيبات آروماتيك را تحريك كند ، اين موضوع براي اكسيمها در سيستمهاي SX هنوز مشاهده نشده است . در مطالب فوق اشاره شد كه نيتراسيون در حضور الكلها اتفاق مي افتد. پس استفاده استخراج كننده هايي كه در فرمول آنها الكل حضور داشته باشد يك ريسك مي باشد.
نيتراسيون درنيترات سديم به تنهايي اتفاق نمي افتد . اين ماده در تركيب الكتروليت هست وباعث كاهش پايداري اكسيم ها مي شود. جالب توجه است كه تبديل مستقيم آلدوكسيم به آلدئيد در حضور نيترات تاليم والكل صورت مي گيرد.
خرید گزارش کامل استخراج مس به روش لیچینگ در مجتمع میدوک شهربابک و مجتمع مس سرچشمه (66 صفحه ،فرمت ورد،قیمت 50 هزار تومان)




